آکسیکرن کی تعداد کو کیسے تلاش کریں

مواد
- مراحل
- حصہ 1 کیمیا کے اصولوں سے آکسیکرن نمبروں کا تعین کرنا
- حصہ 2 ایٹموں کے لئے آکسیکرن کی تعداد کا تعین کریں جو مخصوص اصولوں پر عمل نہیں کرتے ہیں
کیمسٹری میں ، اصطلاح "آکسیڈیشن" اور "کمی" ان رد عمل کا حوالہ دیتے ہیں جس میں بالترتیب ایک ایٹم (یا ایٹموں کا گروہ) الیکٹران کھو جاتا ہے یا حاصل کرتا ہے۔ آکسیکرن نمبر ایٹموں (یا جوہریوں کے گروپ) کو تفویض کردہ نمبر ہیں جو کیمیا دانوں کو یہ جاننے میں مدد دیتے ہیں کہ کتنے الیکٹرانوں کو منتقل کیا جاسکتا ہے اور آیا ایک ریجنٹ کسی رد عمل کے دوران آکسیکرن یا کمی سے گزرتا ہے۔ ایٹموں کے لom ایک ایٹمائزیشن نمبر تفویض کرنے کا عمل جوہری کے انچارج اور انووں کی کیمیائی ساخت پر منحصر ہوتا ہے جو ان سے تعلق رکھتا ہے اس پر منحصر ہے۔ معاملات کو مزید پیچیدہ بنانے کے ل some ، کچھ جوہریوں میں آکسیکرن کی تعداد دو سے زیادہ ہوسکتی ہے۔ خوش قسمتی سے ، آکسیکرن نمبر کا عزم اچھی طرح سے طے شدہ قواعد کے تحت ہوتا ہے جن پر عمل درآمد آسان ہے ، حالانکہ کیمسٹری اور الجبرا کے بارے میں معلومات حاصل کرنا مفید ثابت ہوسکتا ہے۔
مراحل
حصہ 1 کیمیا کے اصولوں سے آکسیکرن نمبروں کا تعین کرنا
-

شناخت کریں کہ جس پروڈکٹ پر آپ کام کر رہے ہیں وہ عنصر کا ایٹم ہے۔ ابتدائی جوہریوں کے آکسیکرن نمبر ، مفت اور دوسرے عناصر کے ساتھ مل کر نہیں ، ہمیشہ 0 ہوتا ہے۔ یہ ان ایٹموں کے لئے درست ہے جن کی ابتدائی شکل اس سادہ ایٹم پر مشتمل ہے ، بلکہ ان ایٹموں کے لئے بھی ہے جن کی ابتدائی شکل ہے diatomic یا پولیٹومیٹک ہے۔- مثال کے طور پر ، Al(S) اور سی ایل2 دونوں کے پاس آکسیکرن کی تعداد 0 ہے کیونکہ وہ بنیادی ، غیرضروری شکل میں ہیں۔
- نوٹ کریں کہ سلفر ، ایس کی بنیادی شکل ہے8، یا آکٹاسلفر ، اگرچہ بے قاعدہ ہے ، میں 0 کا آکسیکرن نمبر بھی ہے۔
-

شناخت کریں کہ آیا سوال میں موجود مصنوعات آئنائزڈ شکل میں ہیں۔ آئنوں کے آکسیکرن کی تعداد ان کے چارج کے برابر ہے۔ یہ آئنوں کے لئے سچ ہے جو دوسرے عناصر سے نہیں جڑے بلکہ آئنوں کے لئے بھی ہیں جو آئنک مرکب کا حصہ ہیں۔- مثال کے طور پر ، کل آئن کا آکسیکرن نمبر -1 ہے۔
- کل آئن کے پاس ہمیشہ جب آکسیڈیشن نمبر -1 ہوتا ہے جب وہ NaCl مرکب کا حصہ ہوتا ہے۔ چونکہ نان آئن کا چارج ، تعریف کے مطابق ، +1 ہے ، ہم جانتے ہیں کہ کل آئن کا چارج -1 ہے۔ اس طرح ، اس کے آکسیکرن کا نمبر ہمیشہ -1 ہوتا ہے۔
-

دھاتی آئنوں کے ل there ، آکسیکرن کی متعدد تعداد ہوسکتی ہیں۔ بہت سے دھات عناصر ایک سے زیادہ بوجھ رکھتے ہیں۔ مثال کے طور پر ، آئرن (Fe) آئنائزڈ شکل میں ہوسکتا ہے +2 یا +3 کے معاوضہ کے ساتھ۔ دھات کے آئنوں کے چارجز (اور اس وجہ سے ان کے آکسیکرن نمبرز) اس بات کا تعین کیا جاسکتے ہیں جس مرکب کے دوسرے جوہری جس کے وہ حصہ ہیں ، یا دوسری صورت میں رومن نمبروں کا استعمال کرتے ہوئے جب یہ معلومات ای کی شکل میں لکھی جاتی ہیں۔ اس جملے میں: "آئرن آئن (III) کا چارج +3 ہے")۔- ایلومینیم میٹل آئن پر مشتمل کمپاؤنڈ کی مثال لیں۔ الکل کمپاؤنڈ3 ہمارا علم ہے کہ سی ایل آئنوں کا چارج -1 ہوتا ہے اور یہ کہ کمپاؤنڈ میں 3 ہوتے ہیں ، لہذا الیون کا چارج +3 ہونا ضروری ہے تاکہ مجموعی طور پر چارج تمام آئنوں میں سے 0 کے برابر ہے۔ لہذا ، آل کی آکسیکرن نمبر +3 ہے۔
-

آکسیجن کو آکسیکرن نمبر -2 (مستثنیات کے ساتھ) تفویض کریں۔ میں سب سے زیادہ کچھ معاملات میں ، آکسیجن ایٹموں میں آکسیکرن کی تعداد -2 ہوتی ہے۔ تاہم ، اس قاعدے میں کچھ استثناء ہیں:- جب آکسیجن بنیادی حالت میں ہوتی ہے (O2) ، اس کا آکسیکرن نمبر 0 ہے ، جیسا کہ تمام ابتدائی ایٹموں کی بات ہے۔
- جب آکسیجن a کا حصہ ہوتا ہے پیروکسائڈ، پھر اس کا آکسیکرن نمبر -1 ہے۔ پیرو آکسائڈس مرکبات کا ایک طبقہ ہے جس میں ایک سادہ آکسیجن آکسیجن (یا پیرو آکسائیڈ آئنون) بانڈ ہوتا ہے2). مثال کے طور پر ، H کے انو میں2اے2 (ہائیڈروجن پیرو آکسائیڈ) ، آکسیجن کی آکسیکرن نمبر (اور اس کا چارج) -1 ہے۔
- جب آکسیجن فلورین کا پابند ہے تو ، اس کا آکسیکرن نمبر +2 ہے۔ مزید معلومات کے ل later ، اس مضمون میں بعد میں فلورائڈ کے اصول پڑھیں۔
-
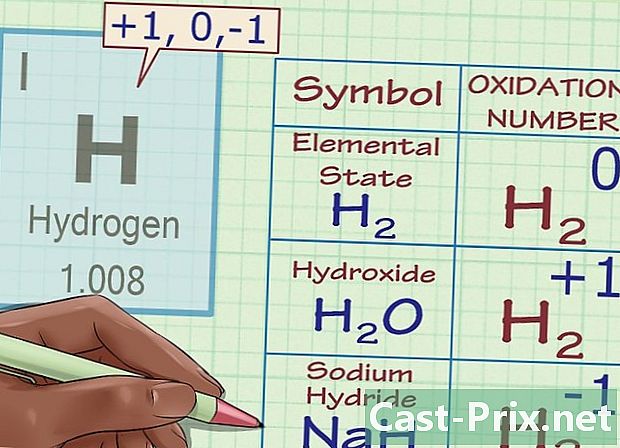
ہائیڈروجن (مستثنیات کے ساتھ) کو آکسیکرن نمبر +1 تفویض کریں۔ آکسیجن کی بات ہے تو ، ہائیڈروجن کے آکسیکرن کی تعداد غیرمعمولی معاملات سے مشروط ہے۔ عام طور پر ، ہائیڈروجن کے آکسیکرن کی تعداد +1 ہے (جب تک کہ ، جب تک کہ وہ اپنی ابتدائی شکل میں نہ ہو ، H2). تاہم ، خصوصی نام نہاد ہائبرڈ مرکبات کی صورت میں ، ہائیڈروجن میں آکسیکرن نمبر -1 ہے۔- مثال کے طور پر ، H کے انو میں2او ، ہم جانتے ہیں کہ ہائیڈروجن میں آکسیڈریشن نمبر +1 ہے کیونکہ آکسیجن کا چارج -2 ہوتا ہے اور ہمیں کمپاؤنڈ کے مجموعی چارج 0 کے ل 2 2 +1 چارجز کی ضرورت ہے۔ تاہم ، سوڈیم ہائیڈرو آکسائیڈ ، ناہ کی ہائبرڈ شکل میں ، ہائیڈروجن میں آکسیکرن کی تعداد -1 ہے کیونکہ نا آئنوں کا +1 چارج ہوتا ہے۔ لہذا ، کمپاؤنڈ کا کل چارج صفر ہونے کے لئے ، ہائیڈروجن چارج (اور اس طرح اس کا آکسیکرن نمبر) -1 کے برابر ہونا چاہئے۔
-

فلور ہے ہمیشہ -1 کا آکسیکرن نمبر۔ جیسا کہ ہم پہلے ہی بیان کر چکے ہیں ، بعض عناصر کے آکسیکرن کی تعداد بہت سے وجوہات کی بناء پر مختلف ہوسکتی ہے (یہ دھات کے آئنوں ، پیروکسائڈز میں آکسیجن ایٹموں کا معاملہ ہے وغیرہ)۔تاہم ، فلورین میں آکسیکرن نمبر -1 ہے ، اور یہ کبھی تبدیل نہیں ہوتا ہے۔ اس حقیقت کی وجہ سے ہے کہ فلورین سب سے زیادہ برقی عنصر ہے - دوسرے لفظوں میں ، یہ وہ عنصر ہے جس کو اپنے الیکٹرانوں میں سے کسی کو دینے کا کم سے کم امکان ہوتا ہے اور اس کا زیادہ تر امکان ہوتا ہے یا کسی اور عنصر کا الیکٹران (زبانیں)۔ اسی لئے اس کا الزام نہیں بدلا جاتا۔ -

کسی کمپاؤنڈ کے آکسیکرن نمبر پر اس کمپاؤنڈ کے معاوضے کے برابر غور کریں۔ کسی مرکب کے تمام ایٹموں کے آکسیکرن نمبروں کا مجموعہ اس احاطے کے معاوضے کے برابر ہونا چاہئے۔ مثال کے طور پر ، اگر کسی مرکب سے معاوضہ نہیں لیا جاتا ہے تو ، اس کے تمام ایٹموں کے آکسیکرن نمبروں کا مجموعہ 0 کے برابر ہونا چاہئے۔ اگر کمپاؤنڈ ایک پولیٹومیٹک چارج آئن -1 ہے تو ، پھر آکسیکرن کی تعداد کا مجموعہ -1 ہونا ضروری ہے۔- یہ چیک کرنے کا ایک اچھا طریقہ ہے کہ آیا آپ نے اپنا کام اچھ .ی انداز میں انجام دیا ہے - اگر آپ کے کمپاؤنڈ کے آکسیکرن نمبروں کا مجموعہ آپ کے احاطے کے کل معاوضے کے برابر نہیں ہے تو آپ کو یقین ہوسکتا ہے کہ آپ نے غلطی کی ہے۔ کہیں آپ کے آکسیکرن نمبروں کا تعین کرنے میں۔
حصہ 2 ایٹموں کے لئے آکسیکرن کی تعداد کا تعین کریں جو مخصوص اصولوں پر عمل نہیں کرتے ہیں
-

ایسے جوہری تلاش کریں جن میں آکسیکرن نمبر تفویض کرنے کے اصول نہیں ہیں۔ کچھ جوہریوں کے ل their ، ان کے آکسیکرن نمبر کے تعین کے لئے کوئی خاص قاعدہ نہیں ہے۔ اگر آپ کا ایٹم سابقہ پیراگراف میں ظاہر نہیں ہوتا ہے اور آپ کو اس کے معاوضہ کا یقین نہیں ہے (مثال کے طور پر یہ کسی بڑے کمپاؤنڈ کا حصہ ہے اور اس کا انفرادی چارج آپ کو نہیں دیا گیا ہے) ، تو آپ کر سکتے ہیں خاتمے کے ذریعہ آگے بڑھ کر ایٹم کے آکسیکرن کی تعداد تلاش کریں۔ پہلے ، آپ اس کمپاؤنڈ کے دوسرے ایٹموں کے آکسیکرن نمبر کا تعین کریں گے ، اس سے پہلے کہ آپ اس کمپاؤنڈ کے مجموعی چارج کی بنیاد پر اس ایٹم کی تعداد کا تعی .ن کریں جو آپ کی دلچسپی ہے۔- مثال کے طور پر ، نا کمپاؤنڈ میں2SO4، سلفر (ایس) کا چارج نامعلوم نہیں ہے - ہم صرف اتنا کہہ سکتے ہیں کہ اس کا چارج 0 سے مختلف ہے کیونکہ وہ اپنی ابتدائی شکل میں نہیں ہے۔ آکسیکرن نمبر کے تعی ofن کے اس الجبری طریقہ کا اطلاق کرنا ایک اچھا امیدوار ہے۔
-

مرکب کے دوسرے عناصر کے آکسیکرن نمبر تلاش کریں۔ آکسیکرن نمبر کا تعین کرنے کے لئے کیمیائی اصولوں کا استعمال کرتے ہوئے ، کمپاؤنڈ کے دوسرے ایٹموں کے آکسیکرن نمبر تلاش کریں۔ O ، H ایٹموں وغیرہ کے غیر معمولی معاملات پر توجہ دیں۔- پچھلے حصے میں بیان کردہ کیمسٹری کے قواعد کے بعد ، ہم جانتے ہیں کہ نا احاطے میں2SO4 نا آئنوں کا چارج (اور اس وجہ سے آکسیکرن نمبر) +1 ہے اور آکسیجن ایٹموں میں آکسیکرن نمبر -2 ہے۔
-

ہر ایٹم کے ل their ، ان کی تعداد کو ان کے آکسیکرن نمبر سے ضرب دیں۔ اب جب کہ ہمیں دلچسپی کے جوہری کے علاوہ اپنے تمام ایٹموں کے آکسیکرن نمبر جانتے ہیں ، لہذا ہمیں اس بات کو ذہن میں رکھنا چاہئے کہ ان میں سے کچھ جوہری مرکبات میں ایک سے زیادہ بار ظاہر ہوسکتے ہیں۔ ہر ایک ایٹم کے عددی گتانک (مرکب میں ایٹم کیمیائی علامت کے بعد انڈیکس میں لکھا ہوا) اس کے آکسیکرن نمبر سے ضرب دیں۔- نا کمپاؤنڈ میں2SO4ہم جانتے ہیں کہ نا کے 2 اور ای کے 4 ایٹم موجود ہیں۔ لہذا ہمیں 2 کا نتیجہ حاصل کرنے کے لئے +1 (نا کے آکسیکرن کی تعداد) کو 2 سے ضرب کرنا ہے ، پھر ضرب کرنا -2 (کی تعداد) -8 کے نتیجہ کو حاصل کرنے کے لئے O کی آکسیکرن 4)۔
-
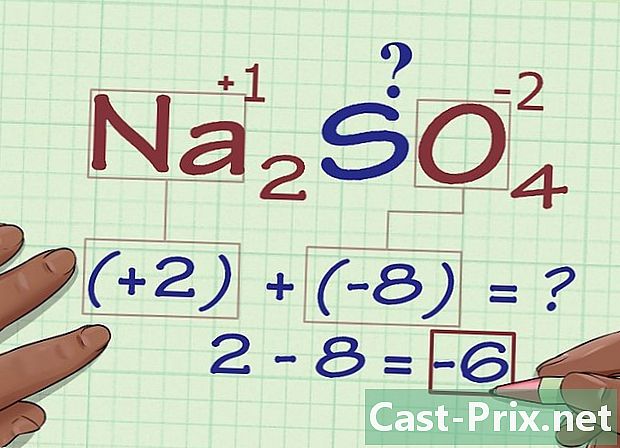
نتائج شامل کریں۔ آکسیکرن نمبر حاصل کرنے کے لئے اپنی ضرب کے نتائج شامل کریں بغیر ایٹم کے آکسیکرن کی تعداد کو جو ہمیں دلچسپی رکھتے ہیں اس کو مدنظر رکھیں۔- نا کی مثال میں2SO4، -6 حاصل کرنے کے لئے 2 اور -8 شامل کرنا ضروری ہوتا۔
-
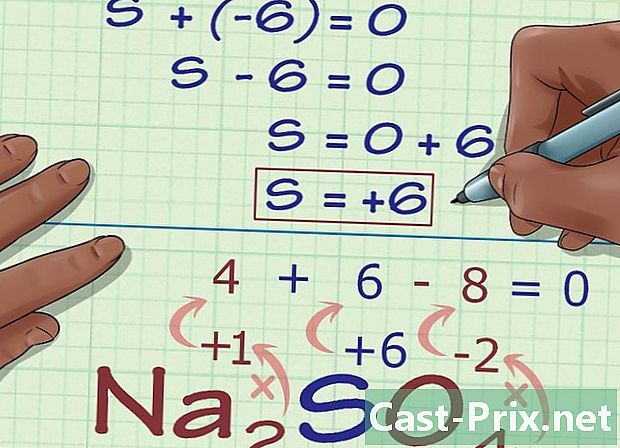
کمپاؤنڈ کے چارج کی بنیاد پر نامعلوم آکسیکرن نمبر کا حساب لگائیں۔ آکسیکرن نمبر تلاش کرنے کے لئے اب آپ کے پاس درکار تمام معلومات موجود ہیں جو آسان الجبری قوانین کا استعمال کرکے ہماری دلچسپی لیتے ہیں۔ ایک ایسی مساوات قائم کریں جس کے مطابق پچھلے مراحل کے علاوہ نامعلوم آکسیکرن نمبر کے نتائج کمپاؤنڈ کے مجموعی چارج کے برابر ہوں گے۔ دوسرے الفاظ میں: (معلوم آکسیکرن نمبروں کا مجموعہ) + (نامعلوم آکسیکرن نمبر) = (مرکب چارج)- نا کی مثال لے کر2SO4یہ کرنے کا طریقہ یہاں ہے:
- (معلوم آکسیکرن نمبروں کا مجموعہ) + (نامعلوم آکسیکرن نمبر) = (مرکب چارج)
- -6 + ایس = 0
- ایس = 0 + 6
- S = 6. S کا آکسیکرن نمبر مساوی ہے 6 نا کمپاؤنڈ میں2SO4.
- نا کی مثال لے کر2SO4یہ کرنے کا طریقہ یہاں ہے:

